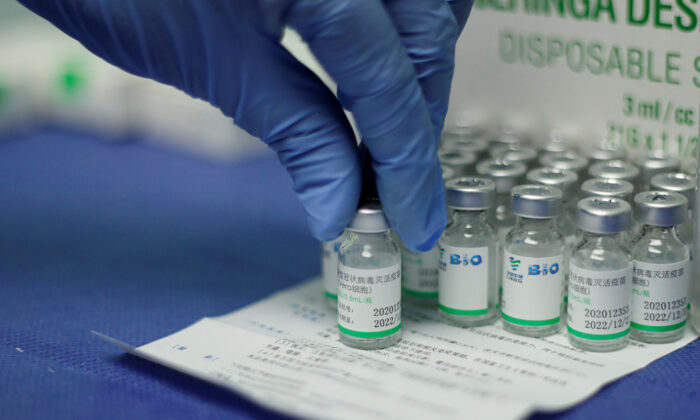
WHO lên tiếng về “độ tin cậy rất thấp” trong một số dữ liệu về vaccine Sinopharm COVID-19

GENEVA – Một tài liệu mà Reuters có được cho thấy, các chuyên gia của WHO đã lên tiếng về “độ tin cậy rất thấp” của dữ liệu do nhà sản xuất dược phẩm quốc doanh của Trung Quốc-Sinopharm-cung cấp liên quan đến nguy cơ mắc các phản ứng phụ nghiêm trọng trên một số bệnh nhân, nhưng nhìn chung vẫn tin tưởng vào khả năng ngăn ngừa bệnh của loại vaccine này.
Một phát ngôn viên của Tổ chức Y tế Thế giới cho biết bản tài liệu về vaccine BBIBP-CorV của Sinopharm này là “một trong nhiều nguồn tài liệu” mà họ dựa vào để đưa ra các khuyến nghị, dự kiến sẽ được công bố vào cuối tuần này.
Tại Bắc Kinh, đã không thể tiếp cận được Sinopharm để nhận được bình luận ngoài giờ làm việc.
Tài liệu “đánh giá bằng chứng” này do Nhóm chuyên gia tư vấn chiến lược của WHO (SAGE) chuẩn bị cho quy trình đánh giá vaccine Sinopharm, vốn đã được 45 quốc gia và khu vực pháp lý chấp thuận sử dụng ở người lớn, với 65 triệu liều đã được chích. Các chuyên gia này sẽ xem xét bằng chứng và đưa ra các khuyến nghị về chính sách và liều lượng liên quan đến vaccine.
Bản tài liệu này bao gồm các tóm tắt dữ liệu từ các thử nghiệm lâm sàng ở Trung Quốc, Bahrain, Ai Cập, Jordan và Các Tiểu vương quốc Ả Rập Thống nhất.
Tài liệu cho biết, hiệu quả của vaccine trong các thử nghiệm lâm sàng Giai đoạn 3 ở nhiều quốc gia là 78.1% sau hai liều. Đây là mức giảm nhẹ so với 79.34% được công bố trước đó ở Trung Quốc.
Tài liệu còn cho biết: “Chúng tôi rất tin tưởng rằng 2 liều BBIBP-CorV là có hiệu quả trong việc ngăn ngừa COVID19 được xác định bằng xét nghiệm PCR ở người lớn từ 18-59 tuổi.
Nhưng trong đó còn có thêm một đoạn: “Việc phân tích mức độ an toàn giữa những người tham gia mắc bệnh nền còn hạn chế vì số lượng ít người tham gia có bệnh lý nền (ngoài bệnh béo phì) trong thử nghiệm lâm sàng giai đoạn 3.”
Trong “khoảng trống bằng chứng,” có trích dẫn dữ liệu về bảo vệ chống lại bệnh nặng, thời gian bảo vệ, độ an toàn khi sử dụng cho phụ nữ có thai và người lớn tuổi và xác định/đánh giá các tác dụng bất lợi hiếm gặp thông qua giám sát an toàn sau khi được chấp thuận.
“Chúng tôi rất ít tin tưởng vào chất lượng của bằng chứng cho thấy nguy cơ xảy ra các tác dụng phụ nghiêm trọng sau một hoặc hai liều BBIBP-CorV ở người lớn tuổi (≥60 tuổi) là thấp.”
“Chúng tôi rất ít tin tưởng vào chất lượng của bằng chứng cho thấy nguy cơ xảy ra các biến cố bất lợi nghiêm trọng ở những người có bệnh lý nền hoặc tình trạng sức khỏe làm tăng nguy cơ mắc COVID-19 nghiêm trọng sau một hoặc hai liều BBIBP-CorV là thấp,” tài liệu này cho biết thêm.
Phân tích SAGE được chuẩn bị khi một nhóm cố vấn kỹ thuật của WHO hiện đang đánh giá xem có thể chấp thuận cho sử dụng khẩn cấp không, điều này không chỉ mở đường cho việc sử dụng vaccine này trong nền tảng chia sẻ vaccine COVAX toàn cầu mà còn cung cấp chứng thực quốc tế quan trọng cho một vaccine được phát triển tại Trung Quốc.
Do Stephanie Nebehay thực hiện
Với sự đóng góp của Reuters
Thu Anh biên dịch
Xem thêm:

 Mới nhất
Mới nhất
 Tiêu điểm
Tiêu điểm
 Bình luận
Bình luận
 Email
Email